网友您好, 请在下方输入框内输入要搜索的题目:
在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是
A.1.8g铝粉和1.8g 铁粉 B.4.2g碳酸镁和2g硝酸银
C.5.6g铁粉和5.6g 锌粉 D.10g碳酸钙和5.6g氧化钙
在20℃时,把甲、乙各10g固体分别加入到两个盛有50g水的烧杯中,充分搅拌,所得甲溶液为24溶液(填饱和或不饱和);若将温度都升高到30℃,甲溶液中溶质的质量分数25 乙溶液中溶质的质量分数(填大于、等于或小于)。
24:不饱和; 25:等于
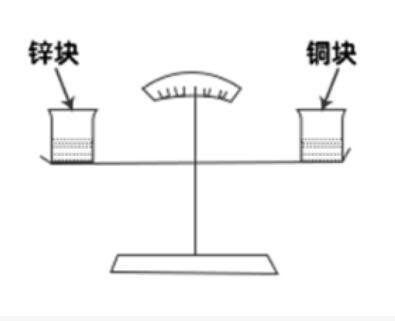
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
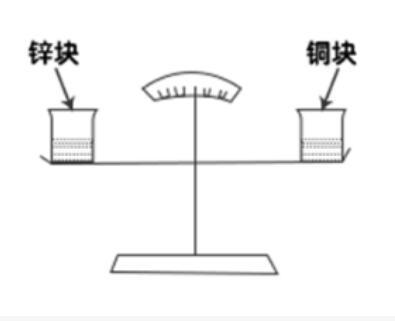
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
现在有一份清漆,成装在烧杯中,烧杯重105克,将该成装清漆的烧杯放在天平上称重显示为195克,在将该清漆放在炉中145℃烘烤25分钟,拿出后放凉称重为145克,计算该清漆的固体份为多少?
正确答案: 清漆重:195-105=80克
烘干后清漆重:145-105=40克
固体份:40÷80×100%=50%
1选择题选择题1、在托盘天平的两盘上各放一只等质量的烧杯,在两只烧杯里分别加入 50g 溶质质量分数为 14.6%的 稀盐酸,将天平调节至平衡。然后向左盘烧杯中投入一定质量的碳酸钠固体,向右盘烧杯中投入 一定质量的镁,均恰好完全反应,天平发生偏转。则下列各项操作中,能使天平重新达到平衡的 是 ( ) 。 A.将游码向右移动 4.2g B.向右盘烧杯中再加入 4g 稀盐酸 C.在右盘上放 4.8g 镁 D在左盘上放 7.2g 碳酸钠固体 2、在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入 50g 溶质质量分数为 7. .3%的稀 盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后, 天平发生偏转的是( ) A1. .8g 铝粉和 1. .8g 铁粉 B4. .2g 碳酸镁和 2g 硝酸银 C5. .6g 铁粉和 5. .6g 锌粉 D10g 碳酸钙和 5. .6g 氧化钙3、将一定量的乙醇和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物 X。测得反应前后物质的质量如下表:物 质乙醇氧气二氧化碳水X反应前质量/g4.68000反应后质量/g004.45.4m下列判断正确的是( )A表中 m 的值为 2.8 BX 可能是该反应的催化剂C增加氧气的量可以减少 X 的生成 D物质 X 一定含有碳元素,可能含有氢元素4、常用燃烧法测定有机物的组成。现取 2.3 g 某有机物在足量的氧气中完全燃烧,生成 4.4 g CO2和 2.7 g H2O。对该物质的组成有下列推断:一定含 C、H 元素 一定不含 O 元素 可能含 O 元素 一定含 O 元素 分子中 C、H 的原子个数比为 2:5 分子中 C、H、O 元素的质量比为 12:3:8。其中正确的是 ( ) A. B. C. D.5、某钢样品的含碳量为 0.24(其他杂质元素不考虑) ,若碳元素主要以 Fe2C 和 Fe3C 的形式存在,则该钢样品中 Fe2C 和 Fe3C 的质量分数()范围是(相对分子质量:Fe2C:124,Fe3C:180)( ) 。A.0.03Cu甲(3)2HgO=2Hg+O2 (合理答案均给分)C+2CuO=2Cu+CO2(合理答案均给分) 用一种金属还原金属氧化物(合理答案均给分)(4)若干燥管内的液(水)面比烧杯内的液(水)面低,且过一段时间后干燥管内的液 (水) 面保持不变充满干燥管 铜片表面有气泡产生,铜片溶解,溶液由无色变成蓝色,液面下降 防止污染空气 解:设生成NO 的质量为 x, 稀硝酸中溶质的质量为 y (设和答共 1 分)3Cu + 8HN03=3Cu(NO3)2 + 2NO + 4H2064*3 8*63 2*303.84g y xx=12g (1 分)y=l008g (1 分)1008g/100g Xl00=1008 (1 分)答:生成 NO 的质量为 12g,稀硝酸中溶质的质量分数为 1008四、基本制备装置正误的识别,装置变形四、基本制备装置正误的识别,装置变形通电 23(1) (2)保证装置的气密性(或“防止生成气体从漏斗逸出” )五、读图、识别装置的能力五、读图、识别装置的能力 (1)O2(或写名称均可) 、补充鱼塘中的氧气、烧杯(2)在水较多的环境中即使生成 CaO,也会和 水作用生成 Ca(OH)2(或其它合理答案均可)实验步骤可能出现的现象结论变红(或产生白色浑浊)CaO2与 H2O 反应有 Ca(OH)2生成取反应后所得的溶液样品滴入酚酞指示剂(或通入 CO2气体)CaO2与 H2O 反应无 Ca(OH)2生成 (3)2CaO22H2O =2Ca(OH)2O2 (4)CaO2与 H2O 的反应是放热反应(意思相近可给分)六、实验六、实验 1、I (1)除去 CO2和 HCl 气体(1 分) (2)验证 CO2是否被除尽(1 分) (3)2.44(2 分) IIABC(答对 2 个给 1 分,全答对给 2 分) (2 分) III97.6%(2 分) 2、 (1)乙 酒精灯 (2)C D G B (3)检查装置气密性3、 (1)木条火焰熄灭(2) 紫色石蕊溶液变红(3) 2NaOH + CO2 =Na2CO3 + H2O 4、 (1)酒精灯 检查装置气密性(2)除去 CO2(3)先撤导管防倒吸(4)C
把30克37%的盐酸配成10%的稀盐酸时所需用的主要仪器是()。
- A、量筒、托盘天平
- B、托盘天平、烧杯、玻璃棒
- C、量筒、烧杯、玻璃棒
- D、量筒、玻璃棒
正确答案:C
称量一定质量NaOH时,下列操作正确的是()。
- A、置于烧杯中在台秤上称量
- B、置于称量纸上于台秤上称量
- C、置于烧杯中在分析天平上称量
- D、置于称量纸上于分析天平上称量
正确答案:A
某学生在用托盘天平测物体质量时,已将天平调好,估计物体质量约20g,将物体和砝码分别放入左右盘中后,发现指针偏向左侧,他应该()。
- A、减少砝码
- B、增加砝码
- C、向左移横梁右端的平衡螺母
- D、向右移横梁右端的平衡螺母
正确答案:B
某同学设计了一种实验方案: 方案:(1)用调节好的天平测出空烧杯的质量m1;(2)向烧杯中倒入一些食用油,测出它们的总质量m2,则这些食用油的质量为m2-m1;(3)再将烧杯中的食用油倒入量筒中,测出食用油的体积V;(4)计算出食用油的密度ρ。 问题: (1)指出该方案的不足之处。 (2)设计教学片段帮助学生改进实验。
正确答案: (1)第三步中,烧杯中液体会倒不干净,会有剩余,测量的质量不准,造成测量出的密度偏小。
(2)师:你的方案总体来说是可行的,但是略有瑕疵。烧杯中的液体倒不干净会怎么样?
生:所测质量会偏小,造成测量密度偏小。
师:但是用烧杯倒液体肯定倒不干净,直接测量不可行,应该怎么办?
生:对!应该采用间接测量的方法。先用天平测出装有适量食用油的烧杯的总质量m1;将烧杯中的一部分食用油倒入量筒中,记录量筒中食用油的体积V;测出烧杯及剩下食用油的总质量m2;这样就可以计算出食用油的密度ρ了。
师:嗯,不错。用这种方案,测量结果误差更小。
在天平的两托盘的烧杯中分别放入相同质量且足量的稀硫酸,调节天平平衡,再往两烧杯中分别加入等质量的Mg和Zn待烧杯中的Mg和Zn全部反应完毕后,天平的指针()。
- A、仍然留在原来的位置
- B、不能停止
- C、偏向Zn的一边
- D、偏向Mg的一边
正确答案:C
更多 “中考化学难题精选+答案” 相关考题
- 2020年以中国为主要贸易伙伴的国家,已经超过百分之多少
- 小张毕业后进入了一家广告公司,凭着过硬的专业素质和不懈的努力很快成为公司的业务骨干,并被提拔为部门经理。但让公司领导略感意外的是,小张升为主管后虽然依然工作勤恳,但他所管理的部门的整体业绩反而较先前有所下降。通过私下询问,员工们普遍反映小张对下属缺乏适当的管理和激励,他似乎并不关心下属的工作绩效问题。问题一:从小张的表现可以看出,他具有较高的( )。 A.亲和需要 B.安全需要 C。权力需要 D.成就需要问题二:具有小张这种较高需要的入,通常有以下特点( )。 A.责任感较弱 B。希望别人顺从自己的意志 C。喜欢得到及时的反馈情况 D.经常选择做有适度风险的工作问题三:根据麦克里兰提出的需要理论,亲和需求高的人常常( )。A。不易受他人影响 B。在组织中充当管理者的角色 C。看重能否被他人接受 D.喜欢能体现其地位的场合
- 形位公差带形状是距离为公差值t的两平行平面内区域的有()A.径向全跳动B.端面全跳动C.平面度D.直线度
- 每一笔贷款只能展期一次.
- 信息化战争涉及的内容包括:A. 信息是核心资源B. 信息化军队C. 信息化、智能化武器装备D. 多维信息化战场E. 信息化战争性质
- ( )是我们后天慢慢习得的一种社会规范和道德,亦即被内化的道德。A.自我B.超我C.本我D.自性
- ( 难度:中等)Hive有哪些方式保存元数据A.derbyB.MySQLC.hdfsD.SQLite
- 论持久战一书发表于多少年。
- ( 难度:中等)MapReduce运行过程包含哪些阶段A.MapB.ReduceC.ShuffleD.Sort
- 本行为收款行,他行为付款行,这类凭证又称为代付票据.